Northern Blotting Technik ist eine Technik, die verwendet wird, um Genexpression zu studieren. Sie wird durch den Befund einer spezifischen RNS (oder des lokalisierten mRNA) durchgeführt. Die mRNA ist in der Regel in 5% der gesamten RNA-Sequenz vertreten. Diese Methode zeigt die Identität, Anzahl, Aktivität und Größe des jeweiligen Gens.

Northern Blotting Technik wird verwendet für
Northern Blotting Technik
Diese Blotting-Technik kann auch für das Wachstum eines Gewebes oder Organismus verwendet werden. In verschiedenen Stadien der Differenzierung und Morphogenese verändert sich die Häufigkeit einer RNA, die mit dieser Technik identifiziert werden kann. Es kann auch abnormale, kranke oder infizierte Zustände auf molekularer Ebene identifizieren. Die Northern-Blot-Technik wurde 1977 von James Alwine, David Kemp und George Stank an der Stanford University entwickelt. Die Technik wurde nach der Ähnlichkeit des Verfahrens mit dem südlichen Blot benannt. Der Hauptunterschied zwischen den beiden Techniken besteht darin, dass im Norden nur RNA an der Färbung beteiligt ist.
Die Subtypen des Blotting, wie Nord, West und Süd, hängen vom gesuchten Zielmolekül ab. Wenn eine DNA-Sequenz die Basis oder der Code für ein Proteinmolekül ist, kann das bestimmte DNA-Molekül von Interesse durch Southern Blotting markiert werden. In der Genexpression, wenn DNS als mRNA für die Produktion eines Proteins ausgedrückt wird, kann dieser Prozess durch Northern Blotting gekennzeichnet werden. Schließlich, wenn die kodierte mRNA das Protein von Interesse produziert, kann diese Proteinidentifizierung durch Western Blotting erfolgen.
Allgemeines Trocknungsverfahren
- Homogenisieren der Probe.
- Trennung des Moleküls von Interesse unter Verwendung einer Elektrophoresemembran.
- Transfer der Moleküle zu einer Nitrocellulose/Nylon-Membran.
- Hybridisierung oder Identifizierung des Moleküls.
Northern Blotting Technique wird verwendet für
Northern Blotting Technik ist eine analytische Technik, die in der Biologie und in der Chemie verwendet wird, um spezifische RNS von einer Mischung von RNAs aufzuspüren. Die Technik wurde 1971 von James Alwine an der Stanford University entwickelt.
In dieser Technik :
- RNAs werden denaturiert, indem H-Bindungen durch die Anwendung von Formaldehyd gebrochen werden (nicht durch die Anwendung einer Restriktionsendonuklease, wie beim Southern Blotting).
- RNAs werden dann auf einer Nylon- oder Nitrocellulosemembran nach Trennung durch Elektrophorese immobilisiert.
- Der Nachweis erfolgt durch radioaktiv markierte Sonden, z. B. P-32, unter einem Autoradiogramm oder nicht radioaktive Sonden (biolumineszent oder enzymgebunden).
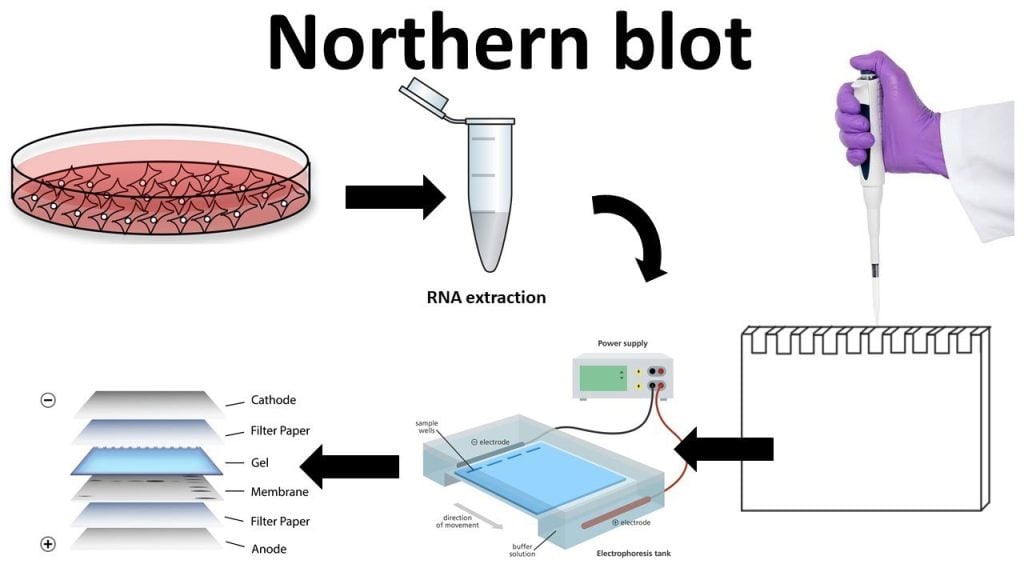
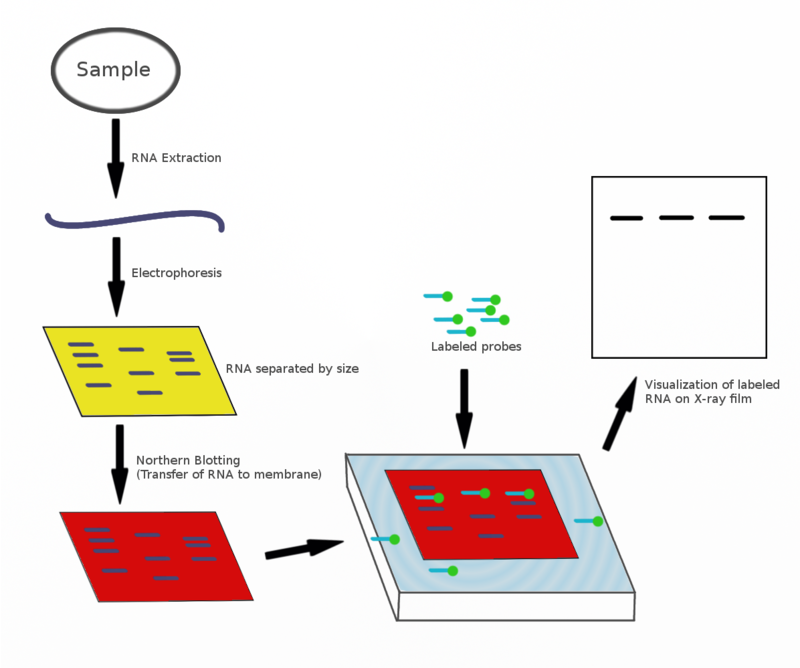
Northern Blotting Schritte
Die Southern-Blotting-Technik besteht aus vier grundlegenden Schritten:
Im ersten Schritt wird die DNA-Probe mit einem Restriktionsenzym aufgespalten oder in kleine Stücke zerlegt. Nach der Verdauung werden die DNA-Fragmente durch Gelelektrophorese getrennt. Dazu wird normalerweise ein Agarosegel verwendet. Die Elektrophorese zeigt mehrere Bänder, die aufgrund der Anwesenheit von mehreren kleinen Restriktionsfragmenten im Gel wie ein Blot aussehen. NaOH wird dann verwendet, um die DNA in einzelne Stränge zu denaturieren.
Diese Bänder werden dann auf die Oberfläche einer Membran unter Verwendung eines elektrischen Gradienten übertragen, der normalerweise ein Blatt Papier ist, das Löschpapier genannt wird. Das Muster der DNA-Fragmente auf dem Gel bleibt nach dem Transfer auf das Löschpapier gleich.
Anschließend wird eine Sonde aus einzelsträngigen DNA-Fragmenten in das Löschpapier eingeführt. Die Basen der DNA-Sonde werden mit komplementären DNA-Sequenzen im Gel gepaart, um die doppelsträngige DNA zu bilden. Die Sonde wird normalerweise mit einem chemischen oder radioaktiven Etikett gekennzeichnet, um die Verfolgung der Sonde im Gel zu ermöglichen. Chemische Substrate und Röntgenfilme werden verwendet, um die Sonde zu lokalisieren, wenn das Etikett ein Enzym ist. Radioaktive Etiketten können direkt auf Röntgenfilmen erscheinen.
Prinzip
Wie alle normalen Blotting-Techniken beginnt das Northern Blotting mit der Elektrophorese, um RNA-Proben nach Größe zu trennen. Elektrophorese trennt RNS-Moleküle entsprechend der Ladung der Nukleinsäuren. Die Ladung der Nukleinsäuren ist proportional zur Größe der Nukleinsäuresequenz.
So trennt die Elektrophoresemembran die Nukleinsäuresequenz entsprechend der Größe der RNS-Sequenz. In Fällen, in denen unsere Zielsequenz eine mRNA ist, kann die Probe durch Oligozellulose-Chromatographie-Techniken isoliert werden, da mRNAs durch den Poly(A)-Schwanz gekennzeichnet werden. Da die Gelmoleküle zerbrechlich sind, werden die getrennten Sequenzen auf Nylonmembranen übertragen. Die Wahl der Nylonmembran ist darauf zurückzuführen, dass Nukleinsäuren von Natur aus negativ geladen sind. Sobald die RNS-Moleküle übertragen werden, werden sie durch eine kovalente Bindung immobilisiert. Die Sonde wird dann hinzugefügt, die Sonde kann komplementär zu einer ssDNA-Sequenz sein. Formamid wird im Allgemeinen als Löschpuffer verwendet, da es die Glühtemperatur senkt.
Northern Blotting Anwendungen
Techniken wie die Real-Time-PCR ermöglichen einen sehr zuverlässigen und schnellen Nachweis auch einer kleinen Sequenz von Targets, während das Southern Blotting eine große Menge an Target-DNA benötigt. Neuere Techniken wie die Fluoreszenz-in-situ-Hybridisierung (FISH) erlauben zudem eine sehr sensitive Identifizierung spezifischer Nukleotidsequenzen in einer Gewebeprobe mit präziser Lokalisation. Real-time PCR und FISH erlauben auch eine genaue Quantifizierung des Targets, was durch Southern Blotting nicht vollständig erreicht werden kann.
Southern Blot hat mehrere Anwendungen im heutigen molekularbiologischen Labor. Einige der Hauptanwendungen von Southern Blot sind
- Identifizierung eines einzelnen Gens in einem Satz von DNA-Fragmenten
- Genkartierung
- Analyse von DNA Gen Mustern
- Nachweis spezifischer DNA-Sequenzen in einem Genom
- die Untersuchung von Gen-Deletionen, Duplikationen und Mutationen, die verschiedene Krankheiten verursachen
- Erkennung genetischer Erkrankungen und Krebserkrankungen wie monoklonale Leukämie und Sichelzellmutationen
- Nachweis des Vorhandenseins einer Genfamilie in einem Genom
- genetische Fingerabdrücke und forensische Tests, wie Vaterschaftstests und Geschlechtsbestimmung.
Western Blot
Western-Blot-Technik bestimmt das Molekulargewicht von Proteinen und misst die Fülle von Proteinen in verschiedenen Proben.
Features Western Blot :
- Nach der Trennung durch Gelelektrophorese unter Verwendung der SDS-PAGE-Methode werden die Proteine auf ein spezielles Löschpapier übertragen, das Nitrocellulose genannt wird, obwohl andere Arten von Papier oder Membranen verwendet werden können. Die Proteine behalten das gleiche Trennmuster wie auf dem Gel.
- Der Blot wird mit einem generischen Protein (z. B. einem Milchprotein) inkubiert, um an klebrige Stellen auf der Nitrocellulose zu binden. Ein Antikörper, der in der Lage ist, an sein spezifisches Protein zu binden, wird dann der Lösung hinzugefügt. Der Antikörper wird zur alkalischen Phosphatase oder zur Meerrettichperoxidase konjugiert.
- Die Position des Antikörpers wird durch Inkubation eines farblosen Substrats aufgedeckt, das das gebundene Enzym in ein farbiges Produkt umwandelt, das gesehen und fotografiert werden kann.
Western Blot (manchmal auch Protein Immunoblot genannt) ist eine weithin anerkannte analytische Technik, die verwendet wird, um spezifische Proteine in einer gegebenen homogenisierten Probe oder in einem Gewebeextrakt zu entdecken. Western-Blot-Proben können aus ganzen Geweben oder aus Zellkulturen entnommen werden. Feste Gewebe werden zunächst mechanisch mit einem Mixer (für große Probenvolumina), einem Homogenisator (für kleine Volumina) oder durch Beschallung gemahlen. Reinigungsmittel, Salze und verschiedene Puffer können verwendet werden, um die Zelllyse zu stimulieren und die Proteine zu lösen.
diese Technik verwendet gelelektrophorese um native Proteine zu trennen entsprechend ihrer dreidimensionalen Struktur oder denaturierten Proteinen entsprechend Polypeptidlänge.

Western Blot Protokoll
Western Blotting (WB) ist eine häufig verwendete Technik in der Molekular- und Zellbiologie sowie im Protein Engineering. Mit einem WB-Assay können Forscher spezifische Proteine aus einer komplexen Mischung von Proteinextraktionen in Zellen trennen und identifizieren. Es gibt drei Hauptteile zu dieser Aufgabe: Trennung nach Molekülgröße, Übertragung auf einen festen Träger durch Gelelektrophorese und Inkubation des Zielproteins mit geeigneten primären und sekundären Antikörpermarkierungen zur Visualisierung.
ARBEITSSCHRITTE FÜR WESTERN BLOTTING:
- Probenvorbereitung: Zelllyse und Proteinextraktion
SDS-PAGE Gel Elektrophorese - Membrantransfer
a) Übergabe aus dem Tank
b) Halbtrocken Transfer - Immunodetection
a) Traditioneller Schutz des Immunoassays
b) 30-minütiges Immunoassay-Protokoll mit SNAP i.d.
c) Immunnachweis des Ganges mit Immobilon GO

Viele Antikörper-Assay-Techniken, wie die indirekte Immunfluoreszenz (IIF) und der enzymgebundene Immunosorbent-Assay (ELISA), wurden in der Vergangenheit entwickelt und überarbeitet. Obwohl diese Methoden empfindlich sind, unterliegen sie auch Kreuzreaktionen, die schwache positive Ergebnisse schwierig zu interpretieren machen.
Unterschied zwischen Southern Northern und Western Blotting
Der Hauptunterschied zwischen der Süd-Nord- und der West-Färbung besteht darin, dass die Süd-Nord-Färbung die Identifizierung von DNA und die Nord-Färbung die Identifizierung von RNA beinhaltet, während die West-Färbung die Identifizierung von Protein beinhaltet.
Süd-, Nord- und West-Blotting sind drei Blot-Techniken, mit denen ein bestimmtes DNA-, RNA- oder Proteinmolekül in einer Probe detektiert wird. Während des Blotting werden Makromoleküle vom Gel auf eine Membran übertragen und binden an eine spezifische Nukleinsäure oder einen Antikörper, der Befund erleichtert.
